
Pro roky 2022 až 2025 byl schválen grant AZV NU22-03-00182 na téma: Prognostický význam cirkulující nádorové DNA u Hodgkinova lymfomu. Hlavní řešitel: Heidi Mociková, spoluřešitelé: Ondřej Havránek, Jan Kořen, Vít Procházka, Alice Sýkorová.
Kromě odběrů na ctDNA u klasického HL ve stanovených intervalech-vždy spolu s vyšetřením PET, se u EBER pozitivních cHL bude odebírat i EBV DNA. Informované souhlasy a pokyny k odběrům ctDNA a EBV DNA a zpracování vzorků krve budou zaslány spoluřešitelům samostatně.
Navrhovaný program pracovní schůze 26.5.2022
- Úvod - H. Móciková
- Výroční zpráva studijní skupiny za rok 2021 - K.Klásková
- Informace o registru HL - Nikola Štourač – projektový manažer HLCZ
- Informace ke grantu AZV NU22-03-00182 – H. Móciková
- Vyšetření TARC u HL - možnosti finanční podpory vyšetření - V. Procházka, H. Móciková
- Plánované prezentace k HL meetingu v Kolíně nad Rýnem - všichni účastníci
- Návrh programu na 7. Mezinárodní sympózium Hodgkinův lymfom v Praze plánovaný na říjen/listopad 2023 - všichni účastníci
- Ostatní - všichni účastníci
63rd ASH Annual Meeting and Exposition (Atlanta, 11-14.12.2021)
V edukační přednášce „Controversies in the management of early-stage Hodgkin lymphoma“ se Kristie A. Blum věnovala možnosti vynechání radioterapie u časných stadií HL na základě interim PET/CT. Ve studiích RAPID, GHSG HD16 a EORTC H10 vynechání radioterapie vedlo ke kratšímu PFS ve srovnání s kombinací chemoradioterapie. Ve studiích RAPID, GHSG HD16 a 17 byli pacienti s Deauville skóre 3 léčeni kombinací chemoterapie a radioterapie, proto je nadále oprávněné používat radioterapii po chemoterapii při dosažené odpovědi při dosažení Deauville skóre 3- po diskusi s pacientem a zvážení potenciálních nežádoucích účinků. Není rozdíl v celkovém přežití mezi skupinami léčenými chemoterapií nebo kombinací chemoterapie a radioterapie.
Hlavním trendem v rámci ASH 2021 bylo hledání optimálního využití brentuximab vedotinu (BV) a checkpoint inhibitorů v první a dalších liniích léčby HL.
První linie léčby.
Kumar a spol. v multicentrické pilotní studii analyzovali možnost vynechání radioterapie u PET –negativních pacientů po 4 cyklech BV s AVD u časných stadií HL s rizikovými faktory. Celkem 114 pacientů bylo rozděleno do čtyř kohort (1.kohorta - 30Gy ISRT, 2.kohorta - 20Gy ISRT, 3.kohorta - 30Gy „consolidation-volume radiotherapy“, 4. kohorta bez radioterapie). Celkový podíl kompletních remisí byl 96 % a 2leté PFS bylo 94 %.
Ve studiích fáze II byl Pembrolizumab použit sekvenčně s AVD (Allen a spol.) nebo souběžně s AVD (Lynch a spol.) zatím na malém počtu pacientů, ale se slibnými výsledky.
Nadále probíhá nábor do studie fáze II SGN 35-027 – ramene C, kde se podávají 4 cykly BV s nivolumabem a chemoterapií AD u časných stadií I-II HL bez bulky masy (Flinn a spol.).
Studie fáze II NIVINHO u pacientů nad 61 let podávala nivolumab +/- vinblastin s celkovou dosaženou odpovědí 51,9 % a 2letým celkovým přežitím 76,7 % (Lazarovici a spol.). Ve studii fáze II se zkouší sekvenční podání dalšího checkpoint inhibitoru Avelumabu s chemoterapií ABVD (Booth a spol.).
Léčba relapsu.
Driessen a spol. retrospektivně srovnávali kombinaci BV a různých chemoterapií oproti samotné chemoterapii. Do analýzy bylo zařazeno 7 studií BV s chemoterapií (celkem 391 pacientů) oproti 2 studiím se samotnou chemoterapií (327 pacientů). 3leté PFS se nelišilo mezi oběma skupinami. V podskupině pacientů s relapsem HL bylo signifikantně lepší 3leté PFS u kombinace BV s chemoterapií oproti chemoterapii samotné. U pacientů s refrakterním HL nebyl rozdíl mezi léčbou s BV nebo bez BV.
Logistická regresní analýza prokázala signifikantně vyšší podíl kompletních metabolických remisí v kohortě BV oproti chemoterapii ICE (73 % vs 61 %), ale signifikantní rozdíl nebyl, pokud se BV a chemoterapie srovnávala se sekvenční chemoterapií ICE-GVD (73% vs 84%).
B symptomy a primární refrakterní HL byly spojené s nižším podílem kompletních metabolických remisí před ASCT.
Kompletní metabolická remise dle PET před ASCT, klinické stadium III/IV, B symptomy a primárně refrakterní HL byli prognostické pro PFS v multivariační analýze.
Desai a spol. v retrospektivní analýze studií s 853 pacienty zjistili, že léčba s checkpoint inhibitory před ASCT vedla k vyššímu podílu kompletních remisí a lepšímu PFS po ASCT ve srovnání se samotnou chemoterapií. Není rozdíl v celkovém přežití po ASCT. Vyšší počet záchranných léčeb před ASCT predikoval nižší PFS a celkové přežití.
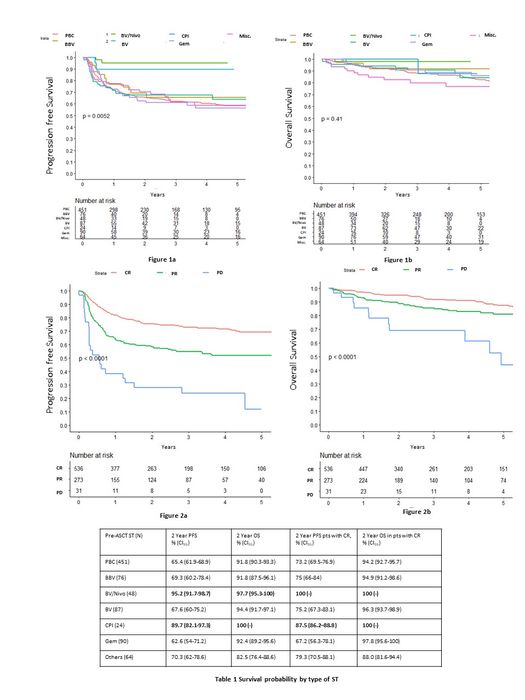
Probíhající multicentrická studie fáze 2b BRESELIBET (Sureda a spol.) srovnává účinnost a bezpečnost 3 cyklů ESHAP v kombinaci s BV oproti 3 cyklům ESHAP. Dalším cílem je zhodnocení účinnosti a bezpečnosti vynechání ASCT, pokud pacienti po 3 cyklech léčby dosáhnou kompletní metabolické remise a dále pokračují v konsolidaci 16 cykly BV.
Epperla a Hamadani v edukační přednášce shrnuli možnosti léčby u pacientů refrakteních na BV a checkpoint inhibitory. Je možné aplikovat chemoterapii na bázi gemcitabinu, platiny, vinca alkaloidů nebo bendamustinu. U mladších pacientů je možnost po dosažení odpovědi na chemoterapii podstoupit alogenní transplantaci kmenových buněk, která dosahuje 3letého celkového přežití 60 %. U pacientů nevhodných k alogenní transplantaci představuje aplikace chemoterapie paliativní postup. Alternativou je experimentální léčba camidanlumab tesirinem, která dosahuje 83 % celkových odpovědí včetně 38 % kompletních remisí. Ostatní léky jako everolimus, lenalidomid, panobinostat mají jen mírný účinek. Experimentálně se zkouší také cytotoxické T lymfocyty anti LMP1 a LMP2 u EBV-pozitivních HL a bispecifická tetravalentní protilátka AFM13.
Léčba pomocí CAR T buněk namířených proti CD30 vede k celkové odpovědi u 62 % pacientů.
MUDr. Heidi Mociková, Ph.D.
Hematologická klinika FNKV a 3.LFUK Praha

